Kandidát na výzkumný lék Lantern Pharma, LP-184, obdržel od FDA druhé zrychlené označení pro léčbu trojnásobně negativního karcinomu prsu (TNBC)
DALLAS--(BUSINESS WIRE) 03. prosince 2024 -- Lantern Pharma Inc. (NASDAQ: LTRN), společnost zabývající se umělou inteligencí (AI), která se věnuje vývoji terapií rakoviny a transformaci nákladů, tempa a časové osy onkologických léků objev a vývoj, dnes oznámila, že FDA udělila Fast Track označení pro testovaný kandidátský lék, LP-184, pro léčbu trojnásobně negativního karcinomu prsu (TNBC). Jedná se o druhé označení Fast Track obdržené pro LP-184 v roce 2024 po jeho označení pro glioblastom v říjnu.
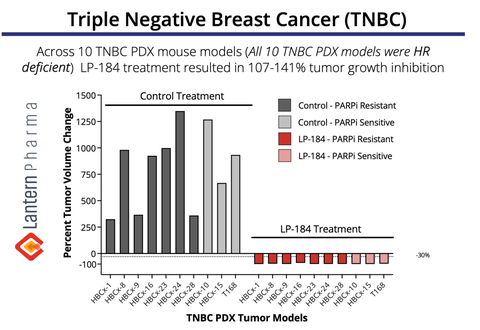
LP-184 prokázal regresi nádoru 107-141 % u více modelů TNBC PDX. (Grafika: Business Wire)
LP-184 je v současné době ve fázi 1A klinické studie navržené k vyhodnocení bezpečnosti a snášenlivosti tohoto synteticky letálního kandidáta na zkoušené léčivo u široké škály pevných nádorů, včetně TNBC. LP-184 byl optimalizován a pokročil částečně s platformou AI společnosti Lantern, RADR®, která pomohla ověřit mechanismy, které by mohly být využity v klinickém prostředí k vymýcení náročných druhů rakoviny a odhalování poznatků v cílové populaci pacientů.
"Příjem". druhé označení FDA Fast Track pro LP-184 posiluje významný potenciál tohoto lékového kandidáta řešit kritické nenaplněné potřeby u agresivních druhů rakoviny, zejména u těch, jako je TNBC, kde pacienti mají omezené terapeutické možnosti,“ uvedla Panna Sharma, prezidentka a generální ředitelka Lantern Pharma. "Nedávné údaje prezentované na Immuno-Oncology Summit prokázaly schopnost LP-184 senzibilizovat nádory TNBC, které nereagují na inhibitory kontrolních bodů, což potenciálně rozšiřuje možnosti léčby pro pacienty s omezenými terapeutickými možnostmi."
O TNBC a potřebě nových terapií
TNBC představuje přibližně 20 % všech případů rakoviny prsu a postihuje ročně téměř 29 000 pacientů v USA. Prognóza pro pacientky s TNBC je podstatně horší než u karcinomů prsu s pozitivními hormonálními receptory, přičemž u více než 50 % pacientek došlo k relapsu v prvních 3–5 letech a pacientky s metastazujícím TNBC mají medián celkového přežití méně než jeden rok. V současnosti dostupné možnosti léčby jsou omezené, zejména u pacientů, u kterých se vyvinula rezistence na stávající terapie.
Přesvědčivé preklinické údaje demonstrují potenciál LP-184 v TNBC
Výše uvedený graf ukazuje pozoruhodnou protinádorovou aktivitu LP-184 na panelu 10 xenoimplantátů získaných od pacienta TNBC ( PDX) modely. Je pozoruhodné, že LP-184 vykazoval konzistentní účinnost jak u PARPi (inhibitor PARP) rezistentních, tak u PARPi citlivých tumorů, přičemž léčba vedla ke kompletní regresi tumoru (107-141% inhibice růstu tumoru) ve všech testovaných modelech. Tato data jsou zvláště významná, protože naznačují potenciál LP-184 jako nové terapeutické možnosti pro pacienty s TNBC, včetně těch, u kterých se vyvinula rezistence na stávající léčbu inhibitory PARP – což je rostoucí klinická výzva v léčbě TNBC. Tato data TNBC byla původně prezentována na Symposiu o rakovině prsu v San Antoniu v roce 2022.
Jedinečný mechanismus účinku LP-184 je řízen enzymatickou aktivací léku prostaglandin reduktázou 1 (PTGR1), která konvertuje LP-184 na jeho vysoce účinnou cytotoxickou formu specificky v rakovinných buňkách. Analýza platformy RADR® a následné validační studie in vivo ukázaly, že PTGR1 je často zvýšený u nádorů TNBC ve srovnání s normální tkání, takže tyto rakoviny jsou zvláště citlivé na léčbu LP-184. Tento přístup založený na biomarkerech umožňuje potenciální identifikaci pacientů, kteří budou s největší pravděpodobností reagovat na terapii LP-184, v souladu se současnými a nově vznikajícími přístupy přesné medicíny v léčbě TNBC.
O LP-184
silný>LP-184 je kandidát na léčivo s malou molekulou a acylfulven nové generace, který přednostně poškozuje DNA v rakovinných buňkách, které nadměrně exprimují specifické biomarkery nebo obsahují mutace v drahách opravy poškození DNA. LP-184 byl vyvinut pomocí vlastní platformy RADR® AI společnosti Lantern k identifikaci populací pacientů a podtypů rakoviny, které mají potenciál reagovat na léčbu. Sloučenina je hodnocena u mnoha pevných nádorů, kde prokázala nanomolární účinnost a aktivitu u rakovin odolných vůči lékům. LP-184 obdržel od FDA označení léku pro vzácná onemocnění pro léčbu rakoviny slinivky břišní, glioblastomu (GBM) a ATRT a také mu bylo uděleno označení pro ATRT pro vzácná dětská onemocnění.
O aplikaci Lantern Pharma
Lantern Pharma (NASDAQ: LTRN) je společnost zabývající se umělou inteligencí, která mění náklady, tempo a časovou osu objevování a vývoje onkologických léků. Naše vlastní platforma AI a strojového učení (ML), RADR®, využívá více než 100 miliard datových bodů zaměřených na onkologii a knihovnu více než 200 pokročilých algoritmů ML, které pomáhají řešit reálné problémy ve vývoji onkologických léků za miliardy dolarů. Využitím síly umělé inteligence a přispěním od špičkových vědeckých poradců a spolupracovníků jsme urychlili vývoj naší rostoucí řady terapií, které zahrnují různé indikace rakoviny, včetně solidních nádorů a rakoviny krve a konjugátu protilátka-lék (ADC ) program. Naše hlavní vývojové programy zahrnují klinický program fáze 2 a několik klinických studií fáze 1. Odhaduje se, že naše řada kandidátů na inovativní produkty řízená umělou inteligencí má kombinovaný roční tržní potenciál přes 15 miliard USD a má potenciál poskytnout život měnící terapie stovkám tisíc pacientů s rakovinou po celém světě.
PROHLÁŠENÍ O PŘEDPOKLADU:
Tato tisková zpráva obsahuje výhledová prohlášení ve smyslu oddílu 27A zákona o cenných papírech z roku 1933 v platném znění a oddílu 21E zákona o burze cenných papírů z roku 1934 v platném znění. Tato výhledová prohlášení zahrnují mimo jiné prohlášení týkající se: budoucích událostí nebo naší budoucí finanční výkonnosti; potenciální výhody naší platformy RADR® při identifikaci kandidátů na léky a populací pacientů, kteří pravděpodobně reagují na kandidáta na lék; naše strategické plány na pokrok ve vývoji našich kandidátů na léky a program vývoje konjugátů protilátek (ADC); odhady týkající se načasování vývoje pro naše kandidáty na léky a vývojový program ADC; očekávání a odhady týkající se načasování klinických studií a náboru pacientů; naše výzkumné a vývojové úsilí našich interních programů pro objevování léků a využití naší platformy RADR® k zefektivnění procesu vývoje léků; náš záměr využít umělou inteligenci, strojové učení a genomická data k zefektivnění a transformaci tempa, rizik a nákladů na objevování a vývoje onkologických léků a k identifikaci populací pacientů, kteří by pravděpodobně reagovali na kandidáta na lék; odhady týkající se populace pacientů, potenciálních trhů a potenciální velikosti trhu; odhady prodeje pro naše kandidáty na léky a naše plány objevit a vyvinout kandidáty na léky a maximalizovat jejich komerční potenciál tím, že takové kandidáty na léky budeme podporovat sami nebo ve spolupráci s ostatními. Jakákoli prohlášení, která nejsou prohlášeními o historické skutečnosti (včetně, bez omezení, prohlášení, která používají slova jako „předvídat“, „věřit“, „uvažovat“, „mohl“, „odhadovat“, „očekávat“, „zamýšlet“, „ hledat, „může“, „může“, „plánovat“, „potenciál“, „předvídat“, „projekt“, „cíl“, „model“, „cíl“, „cíl“, „nadcházející“, „měl by, ""bude," „by“ nebo zápor těchto slov nebo jiné podobné výrazy) by měla být považována za výhledová prohlášení. Existuje řada důležitých faktorů, které by mohly způsobit, že se naše skutečné výsledky budou podstatně lišit od výsledků uvedených v výhledových prohlášeních, jako je (i) riziko, že náš výzkum a výzkum našich spolupracovníků nemusí být úspěšný, (ii) riziko, že pozorování v preklinických studiích a časná nebo předběžná pozorování v klinických studiích nezajistí, že pozdější pozorování, studie a vývoj budou konzistentní nebo úspěšné, (iii) riziko, že v případě potřeby nebudeme schopni zajistit dostatečné budoucí financování a podle potřeby předem a podporu našich stávajících a plánovaných klinických studií a operací, (iv) riziko, že nebudeme úspěšní při licencování potenciálních kandidátů nebo dokončení potenciálních partnerství a spolupráce, (v) riziko, že žádný z našich kandidátů na produkty nezíská marketingový souhlas FDA a nemusíme být schopni úspěšně zahájit, provést nebo uzavřít klinické testování nebo získat marketingové schválení pro naše kandidáty na produkt, (vi) riziko, že žádný lékový produkt založený na naší vlastní platformě RADR® AI nezíská marketingové schválení FDA nebo jinak byly začleněny do komerčního produktu a (vii) tyto další faktory uvedené v části Rizikové faktory v naší výroční zprávě na formuláři 10-K za rok končící 31. prosincem 2023, podané Komisi pro cenné papíry a burzy dne 18. března, 2024. K naší výroční zprávě na formuláři 10-K za rok končící 31. prosincem 2023 se můžete dostat na naší webové stránce v záložce Podklady pro investory SEC na adrese www.lanternpharma.com nebo na webových stránkách SEC na adrese www.sec.gov. Vzhledem k těmto rizikům a nejistotám nemůžeme poskytnout žádné záruky, že se naše výhledová prohlášení ukáží jako přesná nebo že ve skutečnosti nastanou jakékoli jiné výsledky nebo události předpokládané nebo uvažované našimi výhledovými prohlášeními, a varujeme investory, aby neoprávněně se na tato prohlášení spoléhat. Všechna výhledová prohlášení v této tiskové zprávě představují náš úsudek k datu tohoto vydání, a pokud to zákon nevyžaduje jinak, odmítáme jakoukoli povinnost aktualizovat jakákoli výhledová prohlášení tak, aby odpovídala skutečným výsledkům nebo změnám v našich očekáváních. .
Zdroj: Lantern Pharma Inc.
Vyslán : 2024-12-04 06:00
Přečtěte si více

- Nové pravidlo EPA by mohlo uvolnit limity emisí plynů ze sterilizace zdravotnických prostředků
- Průzkum ukazuje, že téměř polovina dětí v USA nemá dostatek spánku
- Společnost Merck oznamuje opožděná data ze tří studií fáze 3 hodnotících doravirin/islatravir (DOR/ISL), výzkumný, jednou denně, dvoulékový režim pro léčbu dospělých žijících s HIV-1 na CROI 2026
- Elektrody částečně obnovují pohyb, pocity u pacientů s míchou
- Velkoobchodní klub BJ vydává Salmon Recall v sedmi státech východního pobřeží
- Kouření mateřského tabáku během těhotenství vázané na vysoký krevní tlak u potomků
Odmítnutí odpovědnosti
Vynaložili jsme veškeré úsilí, abychom zajistili, že informace poskytované na webu Drugslib.com jsou přesné a aktuální -datum a úplné, ale v tomto smyslu není poskytována žádná záruka. Informace o léčivech zde uvedené mohou být časově citlivé. Informace Drugslib.com byly sestaveny pro použití zdravotnickými lékaři a spotřebiteli ve Spojených státech, a proto Drugslib.com nezaručuje, že použití mimo Spojené státy jsou vhodné, pokud není výslovně uvedeno jinak. Informace o drogách na webu Drugslib.com nepodporují léky, nediagnostikují pacienty ani nedoporučují terapii. Informace o lécích na webu Drugslib.com jsou informačním zdrojem, který má pomáhat licencovaným lékařům v péči o jejich pacienty a/nebo sloužit spotřebitelům, kteří tuto službu vnímají jako doplněk, a nikoli náhradu za odborné znalosti, dovednosti, znalosti a úsudek zdravotní péče. praktikující.
Neexistence varování pro daný lék nebo lékovou kombinaci by v žádném případě neměla být vykládána tak, že naznačuje, že lék nebo léková kombinace je pro daného pacienta bezpečná, účinná nebo vhodná. Drugslib.com nepřebírá žádnou odpovědnost za jakýkoli aspekt zdravotní péče poskytované s pomocí informací, které poskytuje Drugslib.com. Informace obsažené v tomto dokumentu nejsou určeny k pokrytí všech možných použití, pokynů, opatření, varování, lékových interakcí, alergických reakcí nebo nežádoucích účinků. Máte-li otázky týkající se léků, které užíváte, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
Populární klíčová slova
- metformin obat apa
- alahan panjang
- glimepiride obat apa
- takikardia adalah
- erau ernie
- pradiabetes
- besar88
- atrofi adalah
- kutu anjing
- trakeostomi
- mayzent pi
- enbrel auto injector not working
- enbrel interactions
- lenvima life expectancy
- leqvio pi
- what is lenvima
- lenvima pi
- empagliflozin-linagliptin
- encourage foundation for enbrel
- qulipta drug interactions
