Lantern Pharma の治験薬候補 LP-184 がトリプルネガティブ乳がん (TNBC) の治療に関して FDA から 2 番目のファストトラック指定を取得
ダラス--(BUSINESS WIRE) 2024 年 12 月 3 日 -- Lantern Pharma Inc. (NASDAQ: LTRN) は、がん治療法の開発と、がん治療薬のコスト、ペース、スケジュールの変革に注力する人工知能 (AI) 企業です。発見と開発の一環として、本日、FDA がトリプルネガティブ乳がん治療用の治験薬候補 LP-184 にファストトラック指定を付与したと発表しました。 (TNBC)。これは、10 月の膠芽腫に対する指定に続き、2024 年に LP-184 が受けた 2 番目のファスト トラック指定となります。
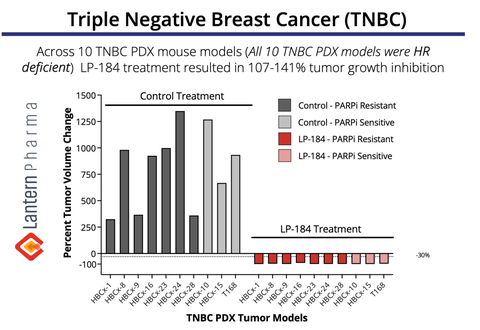
LP-184 は、複数の TNBC PDX モデルで 107 ~ 141% の腫瘍退縮を示しました。 (グラフィック: ビジネスワイヤ)
LP-184 は現在、TNBC を含む広範囲の固形腫瘍におけるこの合成致死性の治験薬候補の安全性と忍容性を評価することを目的とした第 1A 相臨床試験中です。 LP-184 は、Lantern の AI プラットフォームである RADR® の一部を活用して最適化および高度化されており、難題のがんを根絶し、対象となる患者集団の洞察を明らかにするために臨床現場で活用できるメカニズムの検証に役立ちました。
LP-184に対する2度目のFDAファストトラック指定は、悪性度の高いがん、特に患者の治療法が限られているTNBCのようながんにおける重要なアンメットニーズに対処するこの薬剤候補の重要な可能性を強化するものである。オプションです」と Lantern Pharma の社長兼 CEO の Panna Sharma は述べています。 「免疫腫瘍学サミットで発表された最近のデータは、チェックポイント阻害剤に反応しない TNBC 腫瘍を感作する LP-184 の能力を実証し、治療の選択肢が限られている患者の治療選択肢を拡大する可能性があります。」
TNBC と新しい治療法の必要性について
TNBC は全乳がんの約 20% を占め、米国では年間約 29,000 人の患者が罹患しています。 TNBC 患者の予後はホルモン受容体陽性乳がんよりもかなり悪く、患者の 50% 以上が最初の 3 ~ 5 年で再発し、転移性 TNBC 患者の全生存期間中央値は 1 年未満です。現在利用可能な治療の選択肢は限られており、特に既存の治療法に抵抗性を示した患者の場合は限られています。
説得力のある前臨床データは、TNBC における LP-184 の可能性を示しています
上のグラフは、10 個の TNBC 患者由来異種移植片のパネル全体にわたる LP-184 の顕著な抗腫瘍活性を示しています ( PDX)モデル。注目すべきことに、LP-184はPARPi(PARP阻害剤)耐性腫瘍とPARPi感受性腫瘍の両方で一貫した有効性を示し、治療により試験したすべてのモデルで完全な腫瘍退縮(107~141%の腫瘍増殖阻害)が得られました。このデータは、既存のPARP阻害剤治療に耐性を生じた患者を含むTNBC患者(TNBC治療における増大する臨床課題)に対する新たな治療選択肢としてLP-184の可能性を示唆するものであり、特に重要である。この TNBC データは、2022 年のサンアントニオ乳がんシンポジウムで初めて発表されました。
LP-184 の独特の作用機序は、プロスタグランジン レダクターゼ 1 (PTGR1) による薬物の酵素活性化によって引き起こされます。PTGR1 は、特に癌細胞内で LP-184 を非常に強力な細胞傷害性形態に変換します。 RADR® プラットフォーム分析とその後の in vivo 検証研究により、PTGR1 は正常組織と比較して TNBC 腫瘍で頻繁に上昇しており、これらのがんは特に LP-184 治療の影響を受けやすいことが示されています。このバイオマーカー主導のアプローチにより、TNBC 治療における現在および新たな精密医療アプローチと連携して、LP-184 治療に最も反応する可能性が高い患者を特定できる可能性があります。
LP-184 について
強い>LP-184 は、特定のバイオマーカーを過剰発現する、または DNA 損傷修復経路に変異を抱えるがん細胞の DNA に優先的に損傷を与える小分子薬剤候補であり、次世代のアシルフルベンです。 LP-184 は、治療に反応する可能性のある患者集団とがんのサブタイプを特定するために、Lantern 独自の RADR® AI プラットフォームを使用して開発されました。この化合物は複数の固形腫瘍で評価されており、薬剤耐性癌においてナノモルの効力と活性が示されています。 LP-184 は、膵臓がん、神経膠芽腫 (GBM)、ATRT の治療薬として FDA から希少疾病用医薬品指定を受けており、ATRT については希少小児疾患指定も受けています。
概要ランタン製薬
Lantern Pharma (NASDAQ: LTRN) は、腫瘍学の創薬と開発のコスト、ペース、スケジュールを変革する AI 企業です。当社独自の AI および機械学習 (ML) プラットフォームである RADR® は、1,000 億を超える腫瘍学に焦点を当てたデータ ポイントと 200 以上の高度な ML アルゴリズムのライブラリを活用して、腫瘍薬開発における数十億ドル規模の現実世界の問題の解決を支援します。 AI の力を活用し、世界クラスの科学アドバイザーや協力者からの意見を活用することで、当社は固形腫瘍と血液がんの両方、および抗体薬物複合体 (ADC) を含む複数のがんの適応症にわたる成長を続ける治療薬のパイプラインの開発を加速してきました。 )プログラム。当社の主力開発プログラムには、第 2 相臨床プログラムと複数の第 1 相臨床試験が含まれます。 AI を活用した革新的な製品候補のパイプラインは、合計で年間 150 億ドルを超える市場潜在力があると推定されており、世界中の何十万人ものがん患者に人生を変える治療法を提供できる可能性があります。
将来の見通しに関する記述:
このプレスリリースには、1933 年証券法第 27A 条 (改正) および 1934 年証券取引法第 21E 条 (改正) の意味における将来予想に関する記述が含まれています。これらの将来の見通しに関する記述には、特に、以下に関する記述が含まれます。将来の出来事または当社の将来の財務実績。薬剤候補および薬剤候補に反応する可能性が高い患者集団を特定する際の当社の RADR® プラットフォームの潜在的な利点。当社の薬剤候補開発および抗体薬物複合体(ADC)開発プログラムを推進するための戦略的計画。当社の薬剤候補およびADC開発プログラムの開発時期に関する見積もり。臨床試験のタイミングと患者登録に関する期待と推定。社内創薬プログラムの研究開発努力と、創薬プロセスを合理化するためのRADR®プラットフォームの利用。人工知能、機械学習、ゲノムデータを活用して、腫瘍学の創薬と開発のペース、リスク、コストを合理化および変革し、薬剤候補に反応する可能性が高い患者集団を特定するという当社の意図。患者数、潜在的な市場、潜在的な市場規模に関する推定。当社の薬剤候補の売上予測、および薬剤候補を発見および開発し、自社または他者と協力してそのような薬剤候補を開発することでその商業的可能性を最大化する計画。歴史的事実の記述ではないあらゆる記述 (「予想する」、「信じる」、「熟考する」、「可能性がある」、「推定する」、「期待する」、「意図する」、「 「求める」、「かもしれない」、「かもしれない」、「計画する」、「可能性」、「予測する」、「計画する」、「目標とする」、「モデル」、「目的」、「目的」、 「今後の」、「はずである」、「であろう」、「であろう」、またはこれらの言葉の否定語またはその他の同様の表現)は、将来の見通しに関する記述とみなされます。当社の実際の結果が将来の見通しに関する記述で示されたものと大きく異なる原因となる可能性のある重要な要因が多数あります。たとえば、(i) 当社の研究および当社の共同研究者の研究が成功しない可能性があるリスク、(ii)前臨床研究における観察および臨床研究における初期または予備的な観察が、その後の観察、研究、開発の一貫性または成功を保証するものではないリスク、(iii) 必要なときに将来十分な資金を確保できない可能性があるリスク、および既存および計画を推進およびサポートするために必要な場合臨床試験および臨床運営、(iv) 潜在的な候補者へのライセンス供与、または潜在的なパートナーシップや協力関係の完了に成功しないリスク、(v) 当社の製品候補がいずれも FDA のマーケティング承認を受けておらず、当社が承認を受けられない可能性があるリスク当社の製品候補の臨床試験を首尾よく開始、実施、終了することができ、あるいは販売承認を得ることができる、(vi) 当社独自の RADR® AI プラットフォームに基づく医薬品が FDA の販売承認を取得していない、または商業製品に組み込まれていないリスク製品、そして(vii) 2024 年 3 月 18 日に証券取引委員会に提出された、2023 年 12 月 31 日終了年度のフォーム 10-K 年次報告書の「リスク要因」セクションに記載されているその他の要因。当社の年次報告書にアクセスできます。弊社 Web サイト (www.lanternpharma.com) の「投資家向け SEC 提出書類」タブにある、2023 年 12 月 31 日終了年度の Form 10-K またはSEC の Web サイト (www.sec.gov)。これらのリスクと不確実性を考慮すると、当社の将来予想に関する記述が正確であることが証明されるか、または当社の将来予想に関する記述によって予測または検討されているその他の結果や出来事が実際に発生するかについて、当社は保証することができません。これらの記述に過度に依存しないでください。このプレスリリース内のすべての将来予想に関する記述は、本プレスリリースの日付時点での当社の判断を表しており、法律で別段の定めがある場合を除き、当社は、将来予想に関する記述を実際の結果や当社の予想の変化に適合させるために更新する義務を負いません。 .
出典: Lantern Pharma Inc.
投稿しました : 2024-12-04 06:00
続きを読む

- 鎌状赤血球症を専門とする医師の燃え尽き症候群のレベルが上昇
- 米国食品医薬品局、新薬申請を受理し、ナルコレプシー1型に対するファーストインクラスの治療薬候補として武田薬品のオベポレクストン(TAK-861)の優先審査を許可
- 米国FDA、活動性乾癬性関節炎の成人治療薬としてブリストル・マイヤーズ スクイブ社のソティクトゥ(デュクラバシチニブ)を承認
- Chiesi Global Rare Dimensions が、ホモ接合性家族性高コレステロール血症 (HoFH) に対する小児用ジャクスタピド (ロミタピド) カプセルの FDA 承認を発表
- 脂質異常症管理のための ACC/AHA ガイドラインが更新されました
- 新しいガイドラインの詳細 急性肺塞栓症の診断、治療
免責事項
Drugslib.com によって提供される情報が正確であることを保証するためにあらゆる努力が払われています。 -日付、および完全ですが、その旨については保証されません。ここに含まれる医薬品情報は時間に敏感な場合があります。 Drugslib.com の情報は、米国の医療従事者および消費者による使用を目的として編集されているため、特に明記されていない限り、Drugslib.com は米国外での使用が適切であることを保証しません。 Drugslib.com の医薬品情報は、医薬品を推奨したり、患者を診断したり、治療法を推奨したりするものではありません。 Drugslib.com の医薬品情報は、認可を受けた医療従事者による患者のケアを支援すること、および/または医療の専門知識、スキル、知識、判断の代替ではなく補足としてこのサービスを閲覧している消費者にサービスを提供することを目的とした情報リソースです。
特定の薬物または薬物の組み合わせに対する警告がないことは、その薬物または薬物の組み合わせが特定の患者にとって安全、有効、または適切であることを示すものと決して解釈されるべきではありません。 Drugslib.com は、Drugslib.com が提供する情報を利用して管理される医療のいかなる側面についても責任を負いません。ここに含まれる情報は、考えられるすべての使用法、使用法、注意事項、警告、薬物相互作用、アレルギー反応、または副作用を網羅することを意図したものではありません。服用している薬について質問がある場合は、医師、看護師、または薬剤師に問い合わせてください。
人気のあるキーワード
- metformin obat apa
- alahan panjang
- glimepiride obat apa
- takikardia adalah
- erau ernie
- pradiabetes
- besar88
- atrofi adalah
- kutu anjing
- trakeostomi
- mayzent pi
- enbrel auto injector not working
- enbrel interactions
- lenvima life expectancy
- leqvio pi
- what is lenvima
- lenvima pi
- empagliflozin-linagliptin
- encourage foundation for enbrel
- qulipta drug interactions
