Lantern Pharma의 연구용 약물 후보인 LP-184는 삼중 음성 유방암(TNBC) 치료를 위해 FDA로부터 두 번째 신속 지정을 받았습니다.
댈러스--(Business Wire / 뉴스와이어) 2024년 12월 03일 -- 암 치료법을 개발하고 종양학 약물의 비용, 속도, 타임라인을 변화시키는 데 전념하는 인공 지능(AI) 회사인 Lantern Pharma Inc.(NASDAQ: LTRN) 발견 및 개발 회사는 오늘 FDA가 삼중음성유방암(TNBC) 치료를 위한 연구 약물 후보인 LP-184에 대해 패스트 트랙 지정을 부여했다고 발표했습니다. 이는 10월 교모세포종으로 지정된 데 이어 2024년 LP-184가 두 번째로 패스트 트랙 지정을 받은 것입니다.
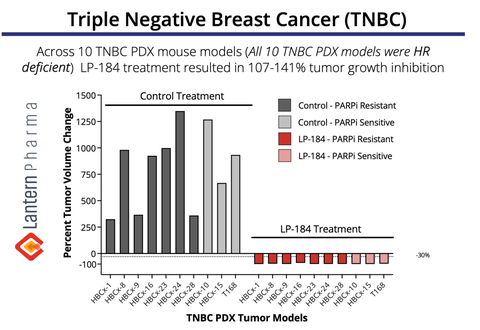
LP-184는 여러 TNBC PDX 모델에서 107-141%의 종양 퇴행을 보여주었습니다. (그래픽: Business Wire)
LP-184는 현재 TNBC를 포함한 광범위한 고형 종양에서 합성 치명적인 연구 약물 후보의 안전성과 내약성을 평가하기 위해 고안된 1A상 임상 시험 중입니다. LP-184는 Lantern의 AI 플랫폼인 RADR®을 통해 부분적으로 최적화되고 발전되었으며, 이는 까다로운 암을 근절하고 표적 환자 집단에서 통찰력을 발견하기 위해 임상 환경에서 활용할 수 있는 메커니즘을 검증하는 데 도움이 되었습니다.
"접수 LP-184에 대한 두 번째 FDA 패스트 트랙 지정은 공격적인 암, 특히 환자가 치료 옵션이 제한적인 TNBC와 같은 암의 중요한 충족되지 않은 요구를 해결할 수 있는 이 약물 후보의 상당한 잠재력을 강화합니다." Lantern Pharma의 사장 겸 CEO인 Panna Sharma입니다. "Immuno-Oncology Summit에서 발표된 최근 데이터는 체크포인트 억제제에 반응하지 않는 TNBC 종양을 민감하게 만드는 LP-184의 능력을 보여주었으며, 치료 선택이 제한된 환자를 위한 치료 옵션을 잠재적으로 확장했습니다."
TNBC 및 새로운 치료법의 필요성
TNBC는 모든 유방암의 약 20%를 차지하며 미국에서 매년 약 29,000명의 환자에게 영향을 미칩니다. TNBC 환자의 예후는 호르몬 수용체 양성 유방암보다 상당히 나쁩니다. 환자의 50% 이상이 처음 3~5년 내에 재발하고 전이성 TNBC 환자의 전체 생존 중앙값은 1년 미만입니다. 현재 이용 가능한 치료 옵션은 제한적이며, 특히 기존 치료법에 내성이 생긴 환자의 경우 더욱 그렇습니다.
강력한 전임상 데이터는 TNBC에서 LP-184의 잠재력을 보여줍니다
위 그래프는 10명의 TNBC 환자 유래 이종이식편 패널에서 LP-184의 놀라운 항종양 활성을 보여줍니다( PDX) 모델. 특히, LP-184는 PARPi(PARP 억제제) 내성 종양과 PARPi 민감성 종양 모두에서 일관된 효능을 나타냈으며, 치료 결과 테스트된 모든 모델에서 완전한 종양 퇴행(107-141% 종양 성장 억제)이 나타났습니다. 이 데이터는 기존 PARP 억제제 치료에 대한 내성이 발생한 환자를 포함하여 TNBC 치료에서 임상적 과제가 증가하고 있는 TNBC 환자를 위한 새로운 치료 옵션으로서 LP-184의 잠재력을 제시한다는 점에서 특히 중요합니다. 이 TNBC 데이터는 2022년 샌안토니오 유방암 심포지엄에서 처음 발표되었습니다.
LP-184의 독특한 작용 메커니즘은 프로스타글란딘 환원효소 1(PTGR1)에 의한 약물의 효소적 활성화에 의해 주도됩니다. PTGR1은 LP-184를 특히 암세포 내에서 매우 강력한 세포독성 형태로 전환시킵니다. RADR® 플랫폼 분석 및 후속 생체 내 검증 연구에 따르면 PTGR1은 정상 조직에 비해 TNBC 종양에서 자주 증가하여 이러한 암이 LP-184 치료에 특히 취약한 것으로 나타났습니다. 이 바이오마커 기반 접근 방식을 통해 TNBC 치료에서 현재 및 신흥 정밀 의학 접근 방식에 맞춰 LP-184 치료에 반응할 가능성이 가장 높은 환자를 식별할 수 있습니다.
LP-184 소개
LP-184는 특정 바이오마커를 과발현하거나 DNA 손상 복구 경로에 돌연변이가 있는 암세포의 DNA를 우선적으로 손상시키는 소분자 약물 후보이자 차세대 아실풀벤입니다. LP-184는 치료에 반응할 가능성이 있는 환자 집단과 암 하위 유형을 식별하기 위해 Lantern의 독점 RADR® AI 플랫폼을 사용하여 개발되었습니다. 이 화합물은 약물 내성 암에서 나노몰의 효능과 활성을 보여준 여러 고형 종양에서 평가되고 있습니다. LP-184는 췌장암, 교모세포종(GBM), ATRT 치료용으로 FDA로부터 희귀의약품 지정을 받았으며, ATRT에 대해서도 희귀소아질환 지정을 받았습니다.
소개 랜턴 제약
Lantern Pharma(NASDAQ: LTRN)는 종양학 약물 발견 및 개발의 비용, 속도, 일정을 변화시키는 AI 회사입니다. 당사의 독점 AI 및 기계 학습(ML) 플랫폼인 RADR®은 1,000억 개가 넘는 종양학 중심 데이터 포인트와 200개 이상의 고급 ML 알고리즘 라이브러리를 활용하여 수십억 달러 규모의 종양학 약물 개발에서 발생하는 실제 문제를 해결하는 데 도움을 줍니다. AI의 힘을 활용하고 세계적 수준의 과학 자문가 및 협력자들의 의견을 바탕으로 우리는 고형 종양과 혈액암, 항체-약물 접합체(ADC)를 비롯한 다양한 암 적응증을 포괄하는 치료제 파이프라인의 개발을 가속화했습니다. ) 프로그램. 당사의 리드 개발 프로그램에는 2상 임상 프로그램과 여러 개의 1상 임상 시험이 포함됩니다. 혁신적인 제품 후보로 구성된 우리의 AI 기반 파이프라인은 연간 총 시장 잠재력이 150억 달러가 넘는 것으로 추산되며 전 세계 수십만 명의 암 환자에게 삶을 변화시키는 치료법을 제공할 수 있는 잠재력을 갖고 있습니다.
미래 예측 진술:
이 보도 자료에는 개정된 1933년 증권법 27A항과 개정된 1934년 증권거래법 21E항의 의미 내에서 미래 예측 진술이 포함되어 있습니다. 이러한 미래 예측 진술에는 무엇보다도 다음과 관련된 진술이 포함됩니다. 미래 사건 또는 당사의 미래 재무 성과; 약물 후보와 약물 후보에 반응할 가능성이 있는 환자 집단을 식별하는 데 있어 당사 RADR® 플랫폼의 잠재적 이점 당사의 약물 후보 및 항체 약물 결합체(ADC) 개발 프로그램 개발을 진전시키기 위한 당사의 전략적 계획; 당사의 약물 후보 및 ADC 개발 프로그램의 개발 시기에 관한 추정치; 임상 시험 시기 및 환자 등록에 관한 기대 및 추정; 내부 약물 발견 프로그램에 대한 연구 및 개발 노력과 약물 개발 프로세스를 간소화하기 위한 RADR® 플랫폼 활용 인공 지능, 기계 학습 및 게놈 데이터를 활용하여 종양학 약물 발견 및 개발의 속도, 위험 및 비용을 간소화 및 변화시키고 약물 후보에 반응할 가능성이 있는 환자 집단을 식별하려는 우리의 의도 환자 인구, 잠재 시장 및 잠재 시장 규모에 관한 추정치; 당사의 신약후보물질에 대한 예상 매출 및 신약후보물질을 발굴 및 개발하고, 해당 신약후보물질을 자체적으로 발전시키거나 다른 업체와 협력하여 상업적 잠재력을 극대화할 계획입니다. 역사적 사실에 대한 진술이 아닌 모든 진술("예상하다", "믿다", "고려하다", "할 수 있다", "추정하다", "기대하다", "의도하다", "와 같은 단어를 사용하는 진술을 포함하되 이에 국한되지 않음) 추구," "할 수 있다", "할 수 있다", "계획", "잠재적", "예측", "프로젝트", "목표", "모델", "목표", "목표", "다가오는", "해야 한다", "할 것이다", "할 것이다" 또는 이러한 단어의 부정문이나 기타 유사한 표현)은 미래 예측 진술로 간주되어야 합니다. (i) 우리의 연구와 협력자의 연구가 성공하지 못할 수 있는 위험, (ii) 전임상 연구의 관찰과 임상 연구의 초기 또는 예비 관찰이 이후의 관찰, 연구 및 개발의 일관성이나 성공을 보장하지 못할 위험, (iii) 필요할 때 향후 충분한 자금을 확보하지 못할 수 있는 위험 기존의 발전과 지원에 필요한 만큼 계획된 임상 시험 및 운영, (iv) 잠재적 후보에 대한 라이선스 부여 또는 잠재적 파트너십 및 협력 완료에 성공하지 못할 수 있는 위험, (v) 제품 후보 중 어느 것도 FDA 마케팅 승인을 받지 못했을 위험, 제품 후보에 대한 임상 테스트를 성공적으로 시작, 수행 또는 결론지을 수 없거나 마케팅 승인을 얻을 수 없는 경우, (vi) 당사의 독점적인 RADR® AI 플랫폼을 기반으로 한 의약품이 FDA 마케팅 승인을 받지 않았거나 다른 방식으로 통합되지 않은 위험 상업용 제품, 그리고 (vii) 명시된 기타 요소들 2024년 3월 18일에 증권거래위원회에 제출된 2023년 12월 31일에 종료된 연도에 대한 양식 10-K의 연례 보고서에 있는 위험 요소 섹션에 나와 있습니다. 해당 연도의 양식 10-K에 대한 연례 보고서에 액세스할 수 있습니다. 당사 웹사이트 www.lanternpharma.com 또는 SEC 웹사이트 www.sec.gov의 투자자 SEC 서류 탭에서 2023년 12월 31일에 종료되었습니다. 이러한 위험과 불확실성을 고려할 때 당사는 당사의 미래 예측 진술이 정확할 것이라는 보장이나 당사의 미래 예측 진술에 의해 예상되거나 고려되는 다른 결과나 사건이 실제로 발생할 것이라고 보장할 수 없습니다. 이 진술에 지나치게 의존하십시오. 본 보도자료에 포함된 모든 미래예측 진술은 보도자료 발행일 현재의 당사의 판단을 나타내며, 법에서 달리 요구하는 경우를 제외하고 당사는 실제 결과나 기대 변화에 맞게 미래예측 진술을 업데이트할 의무가 없습니다. .
출처: Lantern Pharma Inc.
게시됨 : 2024-12-04 06:00
더 읽어보세요

- 약 20개 주에서 HIV 약물 치료 프로그램 축소
- 혈액 검사로 노인의 단기 생존 예측 가능
- AAOS: GLP-1 수용체 작용제 사용으로 골다공증에 대한 5년 위험 증가
- 화이자의 초지속성 주사제 GLP-1 RA PF'3944는 2b상 시험에서 월별 투여로 강력하고 지속적인 체중 감소를 보여줍니다.
- 당신과 당신의 멍청이가 삶에 대해 비슷한 반응을 공유하는 이유
- 짙은 달콤한 체리는 공격적인 유방암을 늦추는 데 도움이 될 수 있다고 생쥐 연구에서 제안합니다
면책조항
Drugslib.com에서 제공하는 정보의 정확성을 보장하기 위해 모든 노력을 기울였습니다. -날짜, 완전하지만 해당 효과에 대한 보장은 없습니다. 여기에 포함된 약물 정보는 시간에 민감할 수 있습니다. Drugslib.com 정보는 미국의 의료 종사자와 소비자가 사용하도록 편집되었으므로 달리 구체적으로 명시하지 않는 한 Drugslib.com은 미국 이외의 지역에서 사용하는 것이 적절하다고 보증하지 않습니다. Drugslib.com의 약물 정보는 약물을 보증하거나 환자를 진단하거나 치료법을 권장하지 않습니다. Drugslib.com의 약물 정보는 면허를 소지한 의료 종사자가 환자를 돌보는 데 도움을 주고/하거나 이 서비스를 건강 관리에 대한 전문 지식, 기술, 지식 및 판단을 대체하는 것이 아니라 보완으로 보는 소비자에게 제공하기 위해 설계된 정보 리소스입니다. 실무자.
특정 약물 또는 약물 조합에 대한 경고가 없다고 해서 해당 약물 또는 약물 조합이 해당 환자에게 안전하고 효과적이거나 적절하다는 의미로 해석되어서는 안 됩니다. Drugslib.com은 Drugslib.com이 제공하는 정보의 도움으로 관리되는 의료의 모든 측면에 대해 어떠한 책임도 지지 않습니다. 여기에 포함된 정보는 가능한 모든 용도, 지시 사항, 주의 사항, 경고, 약물 상호 작용, 알레르기 반응 또는 부작용을 다루기 위한 것이 아닙니다. 복용 중인 약에 대해 궁금한 점이 있으면 담당 의사, 간호사 또는 약사에게 문의하세요.
인기있는 키워드
- metformin obat apa
- alahan panjang
- glimepiride obat apa
- takikardia adalah
- erau ernie
- pradiabetes
- besar88
- atrofi adalah
- kutu anjing
- trakeostomi
- mayzent pi
- enbrel auto injector not working
- enbrel interactions
- lenvima life expectancy
- leqvio pi
- what is lenvima
- lenvima pi
- empagliflozin-linagliptin
- encourage foundation for enbrel
- qulipta drug interactions
