Досліджуваний препарат-кандидат Lantern Pharma, LP-184, отримує другий швидкий дозвіл від FDA для лікування потрійного негативного раку молочної залози (TNBC)
ДАЛЛАС--(BUSINESS WIRE) 3 грудня 2024 р. — Lantern Pharma Inc. (NASDAQ: LTRN), компанія штучного інтелекту (ШІ), яка займається розробкою методів лікування раку та зміною вартості, темпів і графіка онкологічних препаратів відкриття та розробка, сьогодні оголосила, що FDA надало Fast Track Designation для досліджуваного препарату-кандидата, LP-184, для лікування потрійного негативного раку молочної залози (TNBC). Це друге прискорене позначення, отримане для LP-184 у 2024 році, після його позначення для гліобластоми в жовтні.
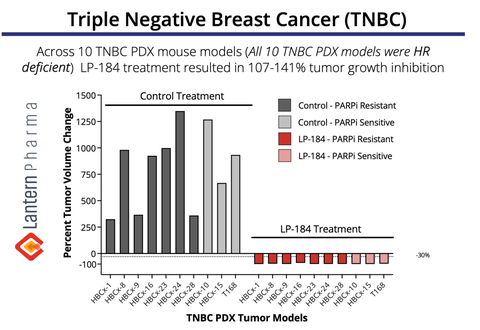
LP-184 продемонстрував регресію пухлини на 107-141% у кількох моделях TNBC. Моделі PDX. (Графіка: Business Wire)
Наразі LP-184 перебуває на стадії клінічних випробувань фази 1А, призначених для оцінки безпеки та переносимості цього синтетично летального досліджуваного препарату для широкого спектру солідних пухлин, включаючи TNBC. LP-184 було оптимізовано та вдосконалено частково за допомогою платформи штучного інтелекту Lantern, RADR®, яка допомогла перевірити механізми, які можна використовувати в клінічних умовах для викорінення складних видів раку та відкриття інформації для цільових груп пацієнтів.
"Отримання друге прискорене призначення FDA для LP-184 підсилює значний потенціал цього препарату-кандидата для вирішення критичних незадоволених потреб при агресивних формах раку, особливо таких, як TNBC, де пацієнти мають обмежені терапевтичні можливості», - заявив Панна Шарма, президент і генеральний директор Lantern Pharma. «Останні дані, представлені на Immuno-Oncology Summit, продемонстрували здатність LP-184 сенсибілізувати пухлини TNBC, які не реагують на інгібітори контрольних точок, потенційно розширюючи можливості лікування для пацієнтів з обмеженим терапевтичним вибором».
Про TNBC та потребу в новій терапії
TNBC становить приблизно 20% усіх випадків раку молочної залози, що вражає майже 29 000 пацієнтів щорічно в США. Прогноз для пацієнтів із TNBC значно гірший, ніж при ракі молочної залози з позитивним гормональним рецептором, причому у понад 50% пацієнтів спостерігається рецидив протягом перших 3-5 років, а пацієнти з метастатичним TNBC мають середню загальну виживаність менше одного року. Наразі доступні варіанти лікування обмежені, особливо для пацієнтів, у яких розвивається стійкість до існуючих методів лікування.
Переконливі доклінічні дані демонструють потенціал LP-184 у TNBC
Наведений вище графік демонструє чудову протипухлинну активність LP-184 на панелі з 10 ксенотрансплантатів TNBC, отриманих пацієнтами ( моделі PDX). Примітно, що LP-184 продемонстрував постійну ефективність як у резистентних до PARPi (інгібіторів PARP), так і в чутливих до PARPi пухлинах, при цьому лікування призвело до повної регресії пухлини (107-141% пригнічення росту пухлини) на всіх протестованих моделях. Ці дані є особливо важливими, оскільки вони свідчать про потенціал LP-184 як нового терапевтичного варіанту для пацієнтів з TNBC, включаючи тих, у кого виникла резистентність до існуючого лікування інгібіторами PARP - зростаюча клінічна проблема в терапії TNBC. Ці дані TNBC були вперше представлені на симпозіумі з питань раку молочної залози в Сан-Антоніо у 2022 році.
Унікальний механізм дії LP-184 обумовлений ферментативною активацією препарату простагландин-редуктазою 1 (PTGR1), яка перетворює LP-184 у його високопотужну цитотоксичну форму саме в ракових клітинах. Аналіз на платформі RADR® і подальші перевірочні дослідження in vivo показали, що PTGR1 часто підвищується в пухлинах TNBC порівняно з нормальною тканиною, що робить ці види раку особливо чутливими до лікування LP-184. Цей підхід, керований біомаркерами, дозволяє потенційно ідентифікувати пацієнтів, які, швидше за все, будуть відповідати на терапію LP-184, узгоджуючи поточні та нові підходи прецизійної медицини до лікування TNBC.
Про LP-184 LP-184 — це маломолекулярний препарат-кандидат і ацилфульвен нового покоління, який переважно пошкоджує ДНК ракових клітин, які надмірно експресують специфічні біомаркери або містять мутації в шляхах відновлення пошкоджень ДНК. LP-184 було розроблено з використанням власної платформи Lantern RADR® AI для визначення популяцій пацієнтів і підтипів раку, які можуть реагувати на лікування. Сполука оцінюється в багатьох солідних пухлинах, де вона показала наномолярну ефективність і активність у стійких до ліків ракових пухлинах. LP-184 отримав від FDA позначення орфанних препаратів для лікування раку підшлункової залози, гліобластоми (GBM) і ATRT, а також отримав позначення рідкісних дитячих захворювань для ATRT. Про Лантерн Фарма Lantern Pharma (NASDAQ: LTRN) – це компанія зі штучним інтелектом, яка змінює вартість, темп і графік відкриття та розробки онкологічних препаратів. Наша запатентована платформа ШІ та машинного навчання (ML) RADR® використовує понад 100 мільярдів точок даних, орієнтованих на онкологію, і бібліотеку з понад 200 передових алгоритмів ML, щоб допомогти вирішити реальні проблеми вартістю мільярд доларів у розробці онкологічних препаратів. Використовуючи можливості штучного інтелекту та внесок наукових консультантів і співробітників світового класу, ми прискорили розробку нашої зростаючої лінійки терапій, які охоплюють численні показання до раку, включаючи як солідні пухлини, так і рак крові та кон’югат антитіло-лікарський засіб (ADC). ) програма. Наші провідні програми розвитку включають клінічну програму Фази 2 і численні клінічні випробування Фази 1. За оцінками, наша серія інноваційних продуктів-кандидатів, керована штучним інтелектом, має сукупний річний ринковий потенціал у понад 15 мільярдів доларів США та потенціал надання терапії, що змінить життя сотням тисяч хворих на рак у всьому світі. ЗАЯВА ПРО МАЙБУТНЄ: Цей прес-реліз містить прогнозні заяви в розумінні розділу 27A Закону про цінні папери 1933 року з поправками та розділу 21E Закону про цінні папери 1934 року з поправками. Ці прогнозні заяви включають, серед іншого, заяви, що стосуються: майбутніх подій або наших майбутніх фінансових показників; потенційні переваги нашої платформи RADR® у визначенні препаратів-кандидатів і груп пацієнтів, які, ймовірно, реагуватимуть на препарат-кандидат; наші стратегічні плани щодо просування розробки наших кандидатів на ліки та програми розробки кон’югатів лікарських засобів з антитілами (ADC); оцінки щодо термінів розробки наших препаратів-кандидатів і програми розробки ADC; очікування та оцінки щодо термінів клінічних випробувань і зарахування пацієнтів; наші дослідження та розробки наших внутрішніх програм відкриття ліків і використання нашої платформи RADR® для оптимізації процесу розробки ліків; наш намір використовувати штучний інтелект, машинне навчання та геномні дані для оптимізації та трансформації темпів, ризиків і вартості відкриття й розробки онкологічних препаратів, а також для визначення популяцій пацієнтів, які, ймовірно, реагуватимуть на препарат-кандидат; оцінки щодо популяції пацієнтів, потенційних ринків і потенційних розмірів ринку; оцінки продажів наших препаратів-кандидатів і наші плани щодо виявлення та розробки препаратів-кандидатів і максимізації їх комерційного потенціалу шляхом просування таких препаратів-кандидатів самостійно або у співпраці з іншими. Будь-які твердження, які не є твердженнями історичного факту (включаючи, без обмежень, твердження, у яких використовуються такі слова, як «передбачити», «вважати», «споглядати», «може», «оцінювати», «очікувати», «має намір», « шукати», «може», «можливо», «планувати», «потенційно», «передбачати», «проектувати», «ціль», «модель», «мета», «мета», «майбутній», «повинен», «буде», «буде» або заперечення цих слів чи інших подібних виразів) слід вважати прогнозними заявами. Існує низка важливих факторів, які можуть призвести до того, що наші фактичні результати суттєво відрізнятимуться від тих, що вказані в прогнозних заявах, наприклад (i) ризик того, що наше дослідження та дослідження наших співавторів можуть бути неуспішними, (ii) ризик того, що спостереження в доклінічних дослідженнях і ранні або попередні спостереження в клінічних дослідженнях не гарантують, що наступні спостереження, дослідження та розробки будуть послідовними або успішними, (iii) ризик того, що ми можемо не мати змоги забезпечувати достатнє фінансування в майбутньому, коли це необхідно та якщо це буде потрібно для просування та підтримки наших існуючих і запланованих клінічних випробувань і операцій, (iv) ризик того, що ми можемо не досягти успіху в ліцензуванні потенційних кандидатів або в завершенні потенційних партнерств і співпраці, (v) ризик що жоден із наших кандидатів на продукт не отримав схвалення FDA на маркетинг, і ми можемо не мати змоги успішно розпочати, провести або завершити клінічне тестування або отримати схвалення на маркетинг для наших кандидатів на продукт, (vi) ризик того, що жоден лікарський продукт, заснований на нашій власній платформі RADR® AI, не отримав схвалення FDA для продажу або іншим чином був включений у комерційний продукт, і (vii) інші фактори, викладені в розділі «Фактори ризику» в нашому річному звіті за формою 10-K. за рік, що закінчився 31 грудня 2023 р., поданий до Комісії з цінних паперів і бірж 18 березня 2024 р. Ви можете отримати доступ до нашого річного звіту у формі 10-K за рік, що закінчився 31 грудня 2023 р., на вкладці «Подання SEC для інвесторів» на нашому веб-сайті www.lanternpharma.com або на веб-сайті SEC за адресою www.sec.gov. Враховуючи ці ризики та невизначеності, ми не можемо гарантувати, що наші прогнозні заяви будуть точними, або що будь-які інші результати чи події, прогнозовані чи передбачені нашими прогнозними заявами, справді відбудуться, і ми застерігаємо інвесторів не надмірно покладатися на ці заяви. Усі прогнозні заяви в цьому прес-релізі представляють наше судження станом на дату цього, і, за винятком випадків, передбачених законом, ми відмовляємося від будь-яких зобов’язань оновлювати будь-які прогнозні заяви, щоб вони відповідали фактичним результатам або змінам наших очікувань. . Джерело: Lantern Pharma Inc. Опубліковано : 2024-12-04 06:00 Було докладено всіх зусиль, щоб інформація, надана Drugslib.com, була точною, до -дата та повна, але жодних гарантій щодо цього не надається. Інформація про ліки, що міститься тут, може бути чутливою до часу. Інформація Drugslib.com була зібрана для використання медичними працівниками та споживачами в Сполучених Штатах, тому Drugslib.com не гарантує, що використання за межами Сполучених Штатів є доцільним, якщо спеціально не вказано інше. Інформація про ліки Drugslib.com не схвалює ліки, не ставить діагноз пацієнтів і не рекомендує терапію. Інформація про ліки на Drugslib.com – це інформаційний ресурс, призначений для допомоги ліцензованим медичним працівникам у догляді за їхніми пацієнтами та/або для обслуговування споживачів, які розглядають цю послугу як доповнення, а не заміну досвіду, навичок, знань і суджень у сфері охорони здоров’я. практиків. Відсутність попередження щодо певного препарату чи комбінації ліків у жодному разі не слід тлумачити як вказівку на те, що препарат чи комбінація препаратів є безпечними, ефективними чи прийнятними для будь-якого конкретного пацієнта. Drugslib.com не несе жодної відповідальності за будь-які аспекти медичної допомоги, що надається за допомогою інформації, яку надає Drugslib.com. Інформація, що міститься в цьому документі, не має на меті охопити всі можливі способи використання, інструкції, запобіжні заходи, попередження, лікарські взаємодії, алергічні реакції чи побічні ефекти. Якщо у вас є запитання щодо препаратів, які ви приймаєте, зверніться до свого лікаря, медсестри або фармацевта.Читати далі

Відмова від відповідальності
Популярні ключові слова
